عام
Les bonnes pratiques de fabrication et les bonnes pratiques de laboratoire

Objectifs de l’enseignement
A la fin du semestre, l'étudiant devra connaître les aspects essentiels de l'assurance et du contrôle qualité appliqués au domaine du médicament et devra pouvoir les mettre en œuvre.
Description de la matière
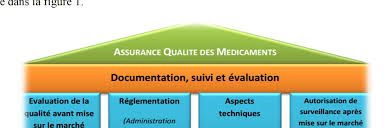
Le cours décrit l’assurance de la qualité comme est un large concept qui couvre tout ce qui peut, individuellement ou collectivement, influencer la qualité d’un produit. Le cours représente les mesures prises pour s’assurer que les médicaments sont de la qualité requise pour l’usage auquel ils sont destinés. L’assurance de la qualité comprend donc les pratiques de fabrication et également d’autres mesures.
Public cible
Ce cours est destiné aux étudiants de master I chimie pharmaceutique.
Pré-requis
Pour suivre ce cours, l’étudiant devra avoir une licence en chimie pharmaceutique ou avoir des connaissances sur les BPF
Plan global du contenu
Ce cours est divisé en huit unités :
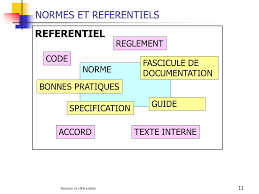
Unité 1 : Définitions – Normes et référentiels
Unité 2 : La certification
Unité 3 : Contexte réglementaire et spécifications pour les spécialités pharmaceutiques et les médicaments pour essais cliniques
Unité 4 : Nouvelles dispositions européennes concernant les GMP (BPF)
Unité 5 : Assurance qualité des produits finis
Unité 6 : Assurance qualité des produits semis-finis en tant que produits finis
Unité 7: Dossier de lot des produits finis
Unité 8: Étiquetage des produits fin
Unité 10: Contexte réglementaire
Unité 11: Les bonnes pratiques du laboratoire
Unité 12: Éventuelles procédures récupération des
produits au cas de réclamation
Unité 13: Procédures De Traitement Des
produits refusés
Références
- Guide des bonnes pratiques de fabrication
- Guide des bonnes pratiques du laboratoire
- Bonnes pratiques de fabrication des produits pharmaceutiques, première partie ( trente deuxième rapport du comité OMS d'experts des spécifications relatives aux préparations pharmaceutiques .Genève, OMS, 1992, annexe 1, série des rapports techniques, N° 823).
- Bonnes pratiques de fabrication : Exigences pour l'échantillonnage des matières premières( trente neuvième rapport du comité OMS d'experts des spécifications relatives aux préparations pharmaceutiques .Genève, OMS, 1992, annexe 2, série des rapports techniques, N° 929).
- Conditionnement des spécialités pharmaceutiques, un élément de choix d'un traitement. La revue prescrite, Août 2011; 334, p 577-578
- Conditionnement des spécialités pharmaceutiques, sécurité et praticité avant tout. La revue prescrite, Octobre 2001; 221, p 701-703
- Agence nationale de sécurité des médicaments et des produits de santé. Rapport d'activité 2013. Août 2014, p 11.
- European medicines agency. Quality Review Of Documents Human Product Information Template. 15 mars 2013, version 9, p 1- 21.
- ....