الحركية الإنزيمية لمادة تفاعل واحدة Cinétique enzymatique à un seul substrat
نموذج الحركة ل Michaélisيسمح بدراسة الخواص الحركية للإنزيمات˛ و تتم الدراسة في المرحلة الثابتة للتفاعل الإنزيميPhase stationnaire de la réaction enzymatique. للبرهان علي معادلة السرعة نتبع الخطوات التالية:
K+1 k+2
E+S ES E+P (1)
k -1 k-2
k+1 = constante de vitesse de la réaction aller E + S (ثابت السرعة للتفاعل الأمامي)
k-1 = constante de vitesse de la réaction ES (ثابت السرعة للتفاعل العكسي)
k+2 = constante de vitesse de la réaction de ES en E + P.
k- 2= constante de vitesse de la réaction de E + P en ES .
تتم دراسة الحركية الإنزيمية في بداية
التفاعل ( بداية المرحلة الثابتة) و عندها يكون تركيز مهمل و الخطوة العكسية غير
مؤثرة علي الحركية و منه يمكن كتابة المعادلة كما يلي:
K+1 K+2
E + S ES E + P (2)
K-1
يمكن
قياس النشاط الانزيمي من خلال تتبع سرعة التفاعل˛ ويمكن حساب السرعة من خلال
العلاقة التالية:
(3) vi =+ d(P) /d(t) ou –d(S)/ d(t)
و بما أن تشكل الناتج أو اختفاء مادة التفاعل يتناسب مع تفكك و تشكيل المعقد الوسطي حسب الحالة فانه يمكن كتابة:
يتكون (ES) في كل لحظة زمنية وفقا لمعدلة من الدرجة الثانية:
E + S ES (5)
و يختفي في كل لحظة و فقا لمعادلتين من الدرجة الأولي:
ES E + S et ES E + P و منه (6) + d(ES) / d(t) = K+1 (E) (S)
-d(ES) /d(t) = k-1 (ES) +K+2 (ES) (7)
بما أن الدراسة تتم في المرحلة الثابتة و التي تتميز ب (8) +d (ES) / d(t) = 0 و منه:
= K+1 (E) (S) (9) k-1 (ES) + K+2 (ES)
اعتمادا علي نظرية المحافظة علي المادة فان: (10) E total = e libre + ES lié
e = Et - ES (11)
نعوض بقيمة المعدلة (11) في (9)
K+1 (S) [(Et - ES)] = k-1 (ES) + K+2 (ES) (12)
K+1 (S) (Et) = K+1 (S) (ES) + k-1 (ES) + K+2 (ES (13)
(ES) = K+1 (S) (Et) / K+1 (S) + ( k-1 (+ K+2 ) (14)
ادا كانت vi = K+2 (ES) (4)
فان Vmax = K+2 (Et) (15)
بقسمة المعادلة (4) علي المعادلة (15) نحصل علي المعادلة التالية:
vi /Vmax =ES/ ET .........16
نعوض بقيمة المعادلة (14) في المعادلة (16)
K+1 (S) (Et)
K+1 (S) + ( k-1 + K+2 ) Vi
Vmx (Et)
بعد الاختصار و تبسيط المعادلة (17) نحصل علي
(18) Vi = Vmax × (S)
Km + (S)
وهي معادلة السرعة ل Michalis et Menten و هي توضح العلاقة بين السرعة و الزيادة في مادة التفاعل.
بحيث Km هو ثابت ميكائيليس و نعبر من خلاله عن جاذبية (S) و (E) حيث يتناسبان عكسيا.
و Vmax تعبر عن السرعة القصوى للتفاعل. و عند هده السرعة تكون جميع المواقع بالإنزيم مشغولة بمادة التفاعل.
يمكن حساب المعايير الحركية للإنزيم انطلاقا من العلاقة التالية :
1- من خلال vi = f(s) Michaelis et Menten (1913):
كما هو موضح في الشكل التالي.
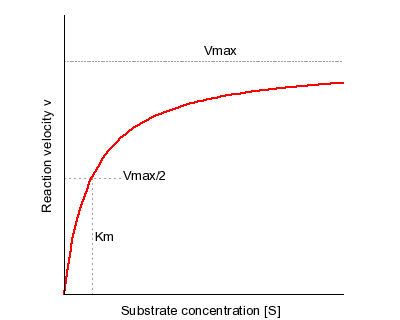
كما يمنكن حساب ثابت ميكائيليس رياضيا من العلاقة التالية: KM = K-1 + k+2 / k+1
2- 1/vi = f (1/S) :Linweaver et Burk(1934)
4- Hanes (1932) : (S) / Vmax = f(S)